Позитронно-эмиссионная томография в практике клинициста
Бойко Д.В., клинический ординатор кафедры госпитальной терапии №2 Челябинской Государственной Медицинской академии. Москва, Декабрь 2006
Позитронно-эмиссионная томография (ПЭТ) – это трехмерный визуализирующий лучевой метод исследования, основанный на способности радиоактивного изотопа накапливаться в тканях, обладающих высокой метаболической активностью.
Наиболее часто используемым изотопом является 2-дезокси-2-[фтор-18]-фторо-D-глюкоза (18-ФДГ ), аналог глюкозы, в котором гидроксильная группа замещена фтором-18.
Период полураспада фтора-18 равен 110 минутам, что значительно больше, нежели у других изотопов, использующихся при ПЭТ.
Так же могут использоваться изотопы: кислород-15 (период полураспада 2 минуты), азот-13 (период полураспада 10 минут) и углерод-11 (период полураспада 20 минут).
Изотопы для ПЭТ производятся в специальных ускорителях элементарных частиц – циклотронах.
Получить изотоп для ПЭТ в простом ядерном реакторе невозможно, поскольку радиоактивная молекула инкорпорируется в биологическую молекулу (в глюкозу, например) для того, чтобы нормально участвовать в физиологических или патологических процессах организма, что невозможно воспроизвести в реакторе.
Из-за избытка протонов в ядре, во время радиоактивного распада эти изотопы излучают позитроны (положительно заряженные электроны), являющиеся формой антиматерии. Позитроны быстро соединяются с электронами, и их масса переходит в энергию.
При каждом таком событии (соединение позитрона и электрона) масса переходит в энергию в виде 2 мощных гамма-лучей или фотонов аннигиляции с энергией 511 кэВ, которые распространяются на 180? друг от друга. Современные ПЭТ-системы способны мгновенно распознавать такие пары фотонов аннигиляции, что и легло в основу концепции т.н. «электрического фазирования».
История вопроса и механизм методики
ПЭТ как метод исследования стала доступна около 20 лет назад – и только сейчас она начинает занимать достойное место среди методов исследования в клинике. Первоначально ПЭТ применялась для диагностики патологии головного мозга и сердца, т.е.
тех локализаций, где были доступны более дешевые методы исследования (рутинное радиоизотопное исследование или УЗИ), где была возможна постановка диагноза клинически (например, при заболеваниях головного мозга) без получения данных о метаболизме в пораженном органе.
В 1990-х годах многие клиницисты стали достойно оценивать ПЭТ как метод, позволяющий поставить диагноз, определить стадию и оценить рецидив при многих злокачественных опухолях из-за высокой тропности изотопа 18-ФДГ к злокачественным клеткам с высокой метаболической активностью.
Захват 18-ФДГ происходит по тому же механизму, что и захват обычной глюкозы, однако захват 18-ФДГ останавливается на этапе фосфорилирования аэробного гликолиза, изотоп соединяется с остатком фосфорной кислоты и остается в клетке.
Это и обеспечивает получение снимков в течение 30-60 минут после инъекции, когда происходит фармакокинетическое распределение препарата по организму.
С конца 1990-х годов ПЭТ стала методикой, которая зарекомендовала себя, что стимулировало быстрый рост популярности и увеличение числа специалистов по ПЭТ среди радиологов, широкое одобрение методики, в особенности среди онкологов.
Появлению рутинной ПЭТ способствовала доступность изотопа 18-ФДГ, чей период полураспада равен 110 минутам, таким образом, изотоп мог быть доставлен в любую клинику на расстояние 100 миль от любого крупного города США.
На Ежегодном Симпозиуме Радиологов в Скоттсдейле в 2002 году была обсуждена настоящая и будущая роль ПЭТ с точки зрения методологии, технического обеспечения и клинической эффективности при многих заболеваниях .
Подготовка пациента к исследованию
Необходим голод в течение 4 часов (или несколько больше). В этот период пациент может употреблять только воду или некалорийные напитки для обеспечения гидратации и увеличения диуреза. Необходимо исследовать уровень глюкозы крови – он не должен превышать 13 ммоль/л.
Высокие уровни глюкозы крови могут снизить захват 18-ФДГ клетками опухоли и ухудшить качество исследования, поэтому следует подумать о повторном проведении исследования, если уровень глюкозы выше 20 ммоль/л.
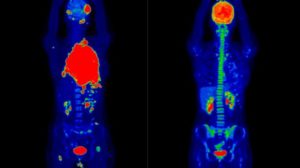
Высокие уровни инсулина вследствие недавнего употребления углеводистой пищи, либо после его экзогенного введения, могут привести к значительному захвату изотопа мышечной тканью, что ухудшает качество исследования (Рисунок 1).
Пациенту следует избегать повышенной физической нагрузки за день до исследования, а после инъекции ФДГ следует расслабиться, прекратить разговаривать, жевать, необходимо избегать гипервентиляции – для того, чтобы минимизировать физиологический захват 18-ФДГ мышечной тканью.
В особенности это касается пациентов с опухолями головы и шеи (необходимо свести к минимуму захват изотопа гортанными и жевательными мышцами). Некоторые авторы рекомендуют использовать бензодиазепины для релаксации мышц [6].
Применение мочегонных и/или катетеризация мочевого пузыря для уменьшения кумуляции изотопа в моче зависит от клинической ситуации и решения врача.
В настоящее время в литературе не сообщается о серьезных побочных эффектах после внутривенного введения 18-ФДГ. После введения изотопа пациент обычно ждет 50-60 минут для более равномерного его распределения в организме, а затем (перед выполнением снимков) мочится для уменьшения кумуляции и повышенной активности изотопа в мочевом пузыре.
И, хотя возможно сделать снимок всего тела за 1 сессию, правильным считается снимок от основания черепа до середины бедра. Рутинное исследование головного мозга не проводится в большинстве центров, поскольку 18-ФДГ относительно нечувствителен к церебральным метастазам, особенно при их небольших размерах.
Нижние конечности снимаются тех случаях, когда есть подозрение на их поражение специфическим процессом. Общее время сканирования зависит от площади изучаемой поверхности, протокола исследования и используемого оборудования. В обычных случаях исследование занимает 1 час (при сканировании от основания черепа до середины бедра) стандартным ПЭТ-сканером.
С недавним введением в практику мерцающего кристалла ускорения LSO и ПЭТ/КТ общее время сканирования снизилось до 30 минут и менее.
Важные анамнестические данные, которые следует выяснить до исследования
Таблица 1 демонстрирует важные данные анамнеза, о которых следует помнить врачу, либо которые необходимо узнать у больного для оптимального ведения пациента и интерпретации данных ПЭТ.
| Подтвержденная или заподозренная беременность, лактация | Прекратить лактацию на 6 часов после введения 18-ФДГ, проанализировать соотношение риск-эффективность ПЭТ при беременности |
| Ранний послеоперационный период/состояние после открытой биопсии | Ожидать повышенного захвата изотопа в месте проведения операции; желательно исследование проводить через 4 недели минимум после операции [9] |
| Недавняя химиотерапия | Возможен измененный захват 18-ФДГ опухолью, возможны реактивные изменения (костный мозг, тимус); желательно проводить ПЭТ через несколько недель после химиотерапии или сразу перед следующим курсом химиотерапии |
| Недавняя лучевая терапия | Возможны постлучевые воспалительные изменения, желательно обеспечить 3-месячный перерыв между лучевой терапией и ПЭТ [9] |
| Применение колониестимулирующих факторов (например, Г-КСФ) | Может быть повышена активность костного мозга; желательно сделать перерыв на несколько недель после последнего назначения Г-КСФ для оптимальной оценки костного мозга |
| Воспалительные процессы (инфекции, абсцессы, саркоидоз) | Хорошо известные случаи ложноположительных результатов ПЭТ; необходима осторожность при трактовке результатов в таких случаях |
| Другие значимые характеристики (клаустрофобия, трудности с положением лежа у пациента | Возможно, потребуется вмешательство или изменение протокола сканирования |
Визуализация, нормальное распределение изотопа и артефакты при сканировании
Ослабление излучения изотопа является большой проблемой ПЭТ, поскольку совокупность путей движения обоих фотонов с энергией 511 кэВ должна по определению «покрывать» всю ширину тела пациента.
Однако эта проблема неплохо решается с помощью коррекционных алгоритмов – программ, которые встраиваются в протокол сканирования. С появлением систем ПЭТ/КТ, вероятно, появятся еще более отработанные коррекционные алгоритмы.
Артефакты при ПЭТ возникают из-за того, что тело человека представляет собой не сферу, а эллипс, поэтому возможны погрешности. Артефакты могут быть обусловлены следующим:
- Движением пациента во время исследования
- Контаминацией из места инъекции
- Предшествующим радионуклидным исследованием (незадолго до ПЭТ)
- Ослаблением излучения и геометрическими искривлениями
- Помехами и погрешностями (плохо отработанная статистическая методика исследования)
- Мышечные артефакты распределения 18-ФДГ
У некоторых больных, которые находятся в состоянии стресса или нервничают во время исследования, возможен аномальный захват 18-ФДГ мышечной тканью. Обычной локализацией такого захвата являются группы мышц шеи, плечевого пояса и верхних конечностей.
Артефакты, обусловленные движением пациента, контаминацией из места инъекции, предшествующими радионуклидными исследованиями, могут быть сведены к минимуму путем простых методик (например, обертывание пациента, обучение пациента перед исследованием, уход). Доктор Barry Siegel из Mallinckrodt Institute of Radiology , г.
Сент-Луис, США заметил, что артефакты, обусловленные геометрическими искажениями, статистическими погрешностями и ослаблением излучения, могут быть несколько уменьшены путем множественных повторяющихся реконструкций изображения (в противоположность старым методам восстановления снимков по их проекциям), в результате чего данные могут быть лучше «подогнаны» к индивидуальным характеристикам пациента.
Нормальный захват 18-ФДГ в значительной степени происходит в головном мозге и мочевом пузыре и, в меньшей степени, в печени, костном мозге и почках. Захват изотопа миокардом может быть неоднородным, что зависит от телосложения пациента и сопутствующей коронарной патологии.
Для снижения захвата изотопа миокардом пациенту необходимо не есть в течение ночи перед утренним исследованием, либо съесть только легкий завтрак, если исследование назначено на вторую половину дня. Доктор Mark W .
Groch из Northwestern University USA доказал, что необходим мониторинг уровня глюкозы крови перед введением 18-ФДГ, целевой уровень – 15 ммоль/л.
Пациенты с уровнем глюкозы более 20 ммоль/л не исследуются, а те, которые имеют уровень глюкозы в пределах 15-20 ммоль/л, подвергаются исследованию только после консультации со специалистами.
Показания к ПЭТ
В основном ПЭТ применяется для диагностики и дифференциальной диагностики злокачественных и доброкачественных опухолей. Главными показаниями для проведения ПЭТ в онкологии являются:
- Диагностика впервые возникших опухолей, в том числе дифференциация доброкачественных опухолей от злокачественных
- Определение стадии заболевания, включая выявление отдаленных метастазов
- Оценка эффективности лечения
- Оценка рецидива заболевания
Однако эти показания для проведения ПЭТ не подходят для всех видов опухолей. В типичных случаях ПЭТ способна выявить очаги поражения размером не менее 7 мм, в редких случаях – 3-4 мм (если ткань очага интенсивно поглощает изотоп).
Стандартные уровни поглощения изотопа ( SUVs – отношение захвата опухолью изотопа к введенной активности) помогают в дифференциальной диагностике злокачественных и доброкачественных опухолей, SUVs при злокачественных опухолях >2,5. Показано, что ПЭТ способна изменять курс лечения при онкологических заболеваниях и избегать ненужных хирургических вмешательств у значительного числа больных.
И хотя применение ПЭТ для оценки состояния головного мозга развивается медленно, выглядит обещающей методика дифференциальной диагностики болезни Альцгеймера от другой патологии головного мозга при помощи ПЭТ.
Доктор David Silverman из UCLA Medical Center , Los Angeles , USA показал, что стандарты клинической диагностики болезни Альцгеймера базируются на устаревшем делении деменций на «излечимые» и «неизлечимые». Тем не менее, некоторые публикации сообщают, что ПЭТ способна поставить диагноз болезни Альцгеймера за 3 года до начала проявления клинических симптомов.
ПЭТ способна четко выявить очаги некроза в миокарде – как самостоятельно, так и в сочетании со сцинтиграфией миокарда. По снимкам можно отличить живой миокард, гибернированный миокард и некроз миокарда.
Показания к применению ПЭТ в онкологии можно представить следующим образом:
| Онкологическое заболевание | Применение ПЭТ |
| Солитарные узлы в ткани легкого | Дифференциальная диагностика злокачественных и доброкачественных новообразований |
| Немелкоклеточный рак легкого | Постановка диагноза, определение стадии, рестадирование |
| Колоректальный рак | Постановка диагноза, определение стадии, рестадирование |
| Лимфома | Постановка диагноза, определение стадии, рестадирование |
| Рак пищевода | Постановка диагноза, определение стадии, рестадирование |
| Меланома* | Постановка диагноза, определение стадии, рестадирование |
| Опухоли головы и шеи** | Постановка диагноза, определение стадии, рестадирование |
| Рак молочной железы*** | Первичная постановка диагноза у больных с отдаленными метастазами Рестадирование у больных с местными рецидивами или отдаленными метастазами Мониторинг ответа на лечение у больных с далеко зашедшей стадией болезни, с отдаленными метастазами, когда планируется смена терапии |
| Рак щитовидной железы | Рестадирование рецидивирующего или остаточного рака щитовидной железы фолликулярного происхождения после тиреоэктомии и лечения радиоактивным йодом, повышенном уровне тиреоглобулина > 10 нг/мл и отрицательном результате сканирования с йодом-131 |
Примечание:
*Исследование регионарных лимфоузлов сюда не относится **Злокачественные опухоли ЦНС не включены
***Диагностика первичного очага опухоли и исследование подмышечных лимфоузлов сюда не включены
Источник: https://mv-scan.ru/pet-issledovanie/pet-kt-protivopokazaniya/
Расшифровка результатов ПЭТ-КТ. Что показывает накопление радиофармпрепарата? | Второе мнение
Физические основы ПЭТ-КТ. Как уже было сказано, ПЭТ-КТ – это сочетание двух методов визуализации – ПЭТ и КТ. ПЭТ основан на введении радионуклидов в человеческий организм, а КТ – на использовании рентгеновского излучения.
Результаты пэт кт
Незадолго до проведения исследования обследуемому вводится радиофармакологический препарат (РФП) – это сочетание радиоизотопа (чаще всего фтор-18, но могут быть и другие, например, углерод-11, азот-13, кислород-15) и биохимического соединения. В роли биохимического вещества обычно используется глюкоза.
Это связано с тем, что глюкоза – это универсальное вещество, которое используется практически всеми клетками человеческого организма и участвует почти во всех процессах.
Также у глюкозы в составе РФП есть одна особенность, также обуславливающая использование в этих целях: дело в том, что универсальный путь обмена глюкозы связан с ее активацией при помощи фермента гексокиназы или глюкозокиназы. При взаимодействии глюкозы с этими ферментами образуется глюкозо-6-фосфат, который в свою очередь расходуется на нужды клетки.
Но если говорить о меченой радиоизотопом глюкозе, то начало будет примерно таким же: РФП, вводимый внутривенно, попадает с током крови в органы и ткани и поглащается там клетками, где происходит его взаимодействие с гексокиназой (глюкозокиназой). В результате этого взаимодействия образуется соединение радиоизотоп-глюкоза-6-фосфат.
На этом этапе с обычной глюкозой взаимодействует другой фермент – глюкозо-6-фосфатдегидрогеназа, но с комплексом радиоизотоп-глюкозо-6-фосфат этот фермент взаимодействовать не может. В результате клетка поглощает РФП и он накапливается в ней. РФП в клетках распадается (по типу бета-распада) с образованием позитрона.
Испускаемый позитрон начинает движение в ткани, но проделывает обычно небольшое расстояние – менее 1 мм. В течение этого времени позитрон теряет кинетическую энергию до того уровня, на котором он сможет взаимодействовать с электроном, в результате чего образуются два фотона, которые движутся в противоположном направлении. Фотоновое излучение в свою очередь фиксируется катушкой томографа, затем данные передаются на компьютер, который выстраивает изображение.
Но на вышеперечисленном технология не заканчивается. Дополнительно визуализацию улучшает использование КТ, что представляет из себя рентгенологический метод послойной визуализации тела человека.
Таким образом, главное преимущество ПЭТ-КТ над использованием ПЭТ и КТ в отдельности – это наложение изображений.
В результате использования ПЭТ-КТ получается изображение, передающее нам данные о морфологии, что достигается использованием КТ составляющей, и о функции органов и тканей и патологии функций на мельчайшем уровне, вплоть до клеточного. При этом мы можем с высокой точностью определить, где произошли изменения и какие это изменения.
Физиологическое накопление рфп при пэт кт
Принципы накопления РФП в организме. Итак, после рассмотрения физического механизма получения изображения, остается понять, почему при одном заболевании получается одна картина, а при другом – совершенно другая, ведь почти все клетки накапливают глюкозу.
Как мы выяснили, томограф фиксирует излучение от РФП, который накапливается в клетках. Но при этом разные клетки в разной степени поглощают глюкозу и, соответственно, РФП: клетки с высоким уровнем обменных процессов будут накапливать РФП в большей степени, с меньшим уровнем – в меньшей, погибшие клетки – вовсе не будут, что бывает, например, в зоне некроза при инфаркте миокарда.
В физиологических условиях следующие ткани поглощают глюкозу, и, как следствие, РФП в большей степени: это ткань головного мозга, скелетная мускулатура, миокард, желудочно-кишечный тракт, почки, а также это может быть жировая ткань (особенно бурый жир). Для этих тканей характерно мягкое диффузное распределение РФП, особенно для скелетной мускулатуры.
В некоторых случаях возможно «ложное» накопление РФП, что бывает при локальных воспалительных процессах, например, абсцессах.
При этом РФП накапливается в патологическом очаге, и, разумеется, это имеет некоторую степень информативности, но данное исследование обычно не проводится с целью выявления абсцессов и тому подобного, следственно это может в некоторых ситуациях только испортить картину.
Второе мнение пэт кт
Итак, РФП накапливается в клетках с преимущественно высоким обменом. Остается выяснить, как это нам поможет в диагностике какой-либо патологии.
И самое первое, это, конечно, онкологические процессы. Опухолевые клетки характеризуются склонностью к неконтролируемому и быстрому делению, а также быстрому росту. Эти процессы требуют постоянного поступления питательных веществ, в том числе глюкозы.
Поэтому опухоли на ПЭТ-КТ характеризуются повышенным накоплением РФП.
И если другие визуализационные методы не всегда могут показать морфологические изменения и степень активности процесса, особенно при малых опухолях, то ПЭТ-КТ позволяет диагностировать рак на сверхранних стадиях, когда никак иначе его не обнаружить.
Также преимуществом ПЭТ-КТ в онкологии является раннее определение метастазов. Особенно, если использовать ПЭТ-КТ сканирование всего тела. Таким способом можно выявить все метастазы, даже самые отдаленные и самые небольшие, и это существенно улучшит качество лечения и, следственно, прогноз.
ПЭТ-КТ позволяет также оценить эффективность проводимой лекарственной химиотерапии и лучевой терапии, так как если терапия эффективна, то размеры опухоли должны уменьшаться, а степень активности процесса снижаться, что отразиться на ПЭТ-КТ томограмме как уменьшение площади накопления и менее интенсивное накопление РФП.
Еще одно специфическое свойство ПЭТ-КТ в онкологии – это дифференцировка между лучевым некрозом окружающей опухоль ткани и прогрессированием опухоли. На КТ разница не всегда будет заметна, а ПЭТ-КТ выявит снижение накопления РФП в ткани в случае некроза, а в случае прогрессирования опухоли – увеличение площади накопления.
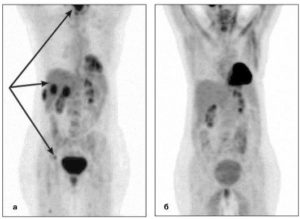
Снимки пэт кт
На данном снимке видны метастазы опухоли в печень, визуализируются даже небольшие по размерам узлы на периферии.
Применение ПЭТ-КТ в неврологии
Как было сказано выше, головной мозг в норме накапливает РФП. Но есть патологические состояния, которые могут снижать накопление РФП в ЦНС.
К таким заболеваниям относится, например, болезнь Альцгеймера. При этом заболевании на ПЭТ-КТ будет отмечаться локальное снижение накопления РФП в больших полушариях, включая кору.
На ПЭТ-КТ изображении видно снижение накопления РФП в височных долях, что в сочетании с клинической картиной позволяет поставить диагноз «болезнь Альцгеймера». Преимуществами ПЭТ-КТ по сравнению с другими методами в диагностике данной болезни являются лучшая визуализация и наличие возможности для ранней диагностики.
Также ПЭТ-КТ позволяет на ранних этапах поставить диагноз болезни Паркинсона, и, что очень важно, другим форм паркинсонизма. Это будет проявляться снижением накопления РФП в подкорковых двигательных ядрах, в частности черной субстанции.
Другие дегенеративные заболевания нервной системы также будут визуализироваться посредством снижения накопления РФП.
Помимо этого, возможна диагностика эпилепсии по данным ПЭТ-КТ. Клетки патологического очага при эпилепсии имеют повышенный обмен даже в межприступный период, что позволяет эффективно обнаружить их и избрать дальнейшую тактику.
Опухоли нервной системы визуализируются на ПЭТ-КТ по принципу других опухолей.
Применение ПЭТ-КТ в кардиологии
Основное состояние, которое может быть эффективно выявлено при помощи ПЭТ-КТ – это гибернация миокарда. Эта форма нарушений кровотока в миокарде не всегда выявляется при помощи других методов визуализации и функциональной диагностики. Участки гибернации характеризуются снижением накопления РФП, как на изображении ниже (участки гибернации выделены синим):
Помимо гибернации миокарда, возможна диагностика и других состояний, например, форм ишемической болезни сердца, не требующих неотложного вмешательства.
Применение ПЭТ-КТ в других сферах
На сегодняшний день существуют данные об использовании ПЭТ-КТ в инфекционных болезнях, при этом используются РФП, имеющие тропность к определенным микроорганизмам, также в клинической фармакологии для определения фармакодинамики и фармакокинетики лекарственных препаратов, некоторых теоретических сферах медицины, но широкого применения и актуальности на данный момент эти сферы применения ПЭТ-КТ не получили.
Источник: https://secondopinions.ru/poleznye-materialy/pet-kt/obschie-voprosy/rasshifrovka-rezultatov-pet-kt-chto-pokazyivaet-nakoplenie-radiofarmpreparata
ПЭТ/КТ в диагностике лимфом
Лимфомы – злокачественные новообразования, исходящие из элементов лимфатических узлов (нодулярная форма) или лимфатической ткани вне их. Они составляют 5% от всех онкологических патологий.
Своевременная диагностика лимфом очень важна не только в связи с высокой распространенностью – заболевание часто встречается у детей и взрослых от 3 до 40 лет, долгое время протекает без выраженных симптомов.
Виды, симптомы и локализация лимфом
Лимфомы разделяют на две большие группы: лимфома Ходжкина (около 60% от всех случаев) и неходжкинские лимфомы, которые являются более агрессивными, прогноз при них хуже. По степени злокачественности неходжкинские лимфомы разделяют на низкую, среднюю и высокую. Одним из самых злокачественных видов болезни является лимфома Беркитта, исходящая из B-лимфоцитов.
Заболевание может развиваться в любом органе или ткани, где есть лимфоидные клетки.
В норме они находятся в лимфоузлах, миндалинах, вилочковой железе, селезенке, фолликулах тонкого кишечника, а также в экстралимфатических органах, не относящихся к лимфатической системе: головном, спинном и костном мозге, легких, матке, яичниках и яичках, почках, печени, желудке, толстом кишечнике, коже и костях.
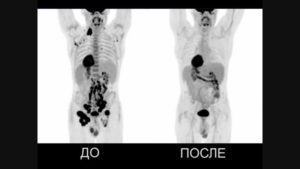
Результаты ПЭТ/КТ-исследования. Слева: неходжкинская лимфома (поражение левой небной миндалины и селезенки, поражение лимфоузлов выше диафрагмы. Справа: ходжкинская лимфома (поражение лимфоузлов по обе стороны от диафрагмы, с тенденцией к слиянию в массивные конгломераты, наиболее крупные в подмышечной области слева и в лимфоузлах средостения справа. III стадия)
На первой-второй стадии заболевания наблюдается ограниченное поражение лимфоузлов или одного экстралимфатического органа по одну сторону диафрагмы – мышечной перегородки между брюшной и грудной полостями. Как правило, самым первым симптомом лимфомы является увеличение лимфатических узлов. Биопсия пораженного лимфоузла и анализ на гистологию позволяют установить правильный диагноз.
На третьей-четвертой стадии выявляется поражение лимфоузлов по обе стороны от диафрагмы и/или нескольких экстралимфатических органов. Пациент жалуется на симптомы, характерные для большинства онкологических болезней: апатию, усталость, похудение, а также на симптомы, связанные с поражением конкретного органа.
Для выбора адекватной терапии при лимфомах важно:
- комплексное обследование до начала терапии: определение вида, степени злокачественности и стадии болезни у пациента с поставленным диагнозом;
- своевременно контролировать эффективность терапии: на промежуточных этапах между курсами для определения эффективности выбранной схемы и своевременной корректировки плана лечения, а также после полного курса для определения риска рецидива или подтверждения ремиссии заболевания.
Наиболее информативным методом определения стадии и агрессивности заболевания является ПЭТ/КТ. КТ и МРТ также используют для диагностики, но с их помощью сложно отличить злокачественный процесс от доброкачественных изменений, а оценка распространенности процесса занимает больше времени, чем при ПЭТ/КТ.
Позитронно-эмиссионная томография позволяет провести анализ метаболических процессов в клетках.
Злокачественные опухоли поглощают питательные вещества интенсивнее обычных, это значит, что они накапливают больше радиофармпрепарата и хорошо видны на снимках как участки яркого свечения.
КТ и МРТ показывают только структурные изменения органов, объективно оценить функциональное состояние клеток этими методами невозможно.
ПЭТ/КТ всего тела у пациентов с лимфомами
Для обследования пациентов с лимфомами применяют ПЭТ/КТ всего тела с 18F-фтордезоксиглюкозой. Этот радиопрепарат распространяется по всем органам и тканям. За одно исследование врач получает изображение всех анатомических областей. Для достижения такого охвата при диагностическом КТ нужен анализ серии исследований различных областей тела, что увеличивает лучевую нагрузку на пациента.
ПЭТ/КТ при лимфомах применяют в следующих случаях:
- определение стадии опухолевого процесса и степени его распространенности;
- анализ эффективности лечения, в том числе на ранних этапах;
- уточнение прогноза заболевания;
- планирование лучевой терапии;
- определение лучшего участка для биопсии;
- диагностика рецидивов болезни.
По различным данным чувствительность ПЭТ/КТ диагностики может достигать 100% при диффузной В-крупноклеточной лимфоме, 98% при лимфоме Ходжкина и фолликулярной лимфоме, 67% при формах, поражающих зону мантии, 95% при миеломной болезни. Обследование наиболее результативно в случаях, когда клетки лимфомы характеризуются повышенной активностью, то есть при болезни Ходжкина и неходжкинских лимфомах высокой степени злокачественности.
Вы можете задать вопрос о применении ПЭТ/КТ-диагностики
при лимфоме нашим ведущим специалистам: Абашин Сергей Юрьевич, д.м.н., профессор, врач-онколог, врач-химиотерапевт, г. Москва Ручьева Наталья Александровна, к.м.н., зав. отделением радионуклидной диагностики, рентгенолог-радиолог, г. Москва Иванников Виталий Валерьевич, руководитель направления «Лучевая диагностика», рентгенолог-радиолог, г. Москва
Первичная диагностика и определение стадии лимфом
В настоящее время лимфомы, особенно лимфома Ходжкина, относятся к злокачественным заболеваниям с хорошим прогнозом.
После гистологической верификации диагноза нужно точно определить стадию и степень злокачественности заболевания.
Для правильного выбора схемы химиотерапии надо знать, насколько опухоль распространилась по телу и лимфоузлам, а для назначения радиотерапии важно точное местоположение опухоли.
ПЭТ/КТ позволяет выявить злокачественные опухоли от 6 мм в диаметре и точно измерить метаболический размер очага.
Часто первичная диагностика проводится с помощью рентгенографии, УЗИ, КТ, МРТ, а схема лечения подбирается на основе количества и размера выявленных очагов.
Вокруг злокачественных опухолей по мере ответа на лечение часто образуется соединительная ткань или происходит некроз опухолевых тканей из-за нарушения кровообращения. Такие процессы становятся причиной ошибок при анализе размеров очага – он кажется больше, чем есть на самом деле.
Также КТ и МРТ могут пропустить новообразования в случаях, когда патологический процесс происходит на клеточном уровне, и структура органа или лимфоузла визуально не изменяется.
ПЭТ/КТ позволяет выявить злокачественные опухоли от 6 мм в диаметре и точно измерить метаболический размер очага. На снимке видны активные злокачественные клетки, а соединительная ткань почти не отличается от здоровых участков, так как не поглощает радиофармпрепарат.
ПЭТ/КТ для анализа эффективности лечения
Проведение ПЭТ/КТ-исследования, г. Москва
Для анализа эффективности лечения лимфомы важно оценить скорость реакции опухоли на терапию.
Если количество активных клеток в очагах снижается до минимума или они исчезают полностью – это считается полным метаболическим ответом. У пациентов с таким ответом в короткие сроки (после 2-3 курса) наблюдаются более длительные ремиссии.
В противном случае, когда число активных клеток не уменьшается или растет – пациенту требуется коррекция схемы лечения.
С помощью КТ или МРТ сложно подтвердить или опровергнуть достижение ремиссии, в 30-60% случаев устанавливают неверный диагноз.
Дело в том, что на месте опухолевого очага у ряда пациентов остается соединительная ткань, лимфоузлы могут замещаться ей полностью (фиброз). Участки фиброза при КТ или МРТ исследовании видны как структурное изменение органа.
Только позитронно-эмиссионная томография помогает увидеть, остались ли в таких очагах активные злокачественные клетки.
В результате ПЭТ/КТ позволяет повысить эффективность лечения и улучшить прогноз:
- своевременный перевод пациентов, опухоль которых не реагирует на лечение, на высокодозную химиотерапию или назначение им лучевой терапии повышает шансы на выживание;
- снижение интенсивности терапии, отказ от высоких доз химиопрепаратов или лучевого лечения у пациентов с ремиссией уменьшает риск осложнений и увеличивает выживаемость в долгосрочной перспективе.
Цены на ПЭТ/КТ исследование в Москве
Цены на позитронно-эмиссионную томографию в Москве зависят от вида исследования. Стоимость вы можете уточнить по телефону круглосуточной информационно-справочной службы или посмотреть в прайс-листе.
Федеральная сеть центров ядерной медицины «ПЭТ-Технолоджи» оказывает пациентам диагностическую и лечебную помощь в соответствии с международными стандартами качества.
Целесообразность проведения ПЭТ/КТ в каждом конкретном случае заболевания лимфомой определяет врач-гематолог.
Наши центры в Москве и других городах оснащены современным оборудованием для ПЭТ/КТ диагностики, в штате работают квалифицированные врачи-радиологи, прошедшие стажировку в ведущих медицинских клиниках и диагностических учреждениях России и мира.
Часто задаваемые вопросы о ПЭТ/КТ
Источник: https://www.pet-net.ru/pet-kt-diagnostika/limfoma.php
Диагностика рака лимфоузлов
Диагностика рака лимфоузлов необходима для стадирования процесса, оценки тяжести состояния пациента, и определения морфологического типа опухоли.
Методы диагностики рака лимфоузлов могут быть следующие:
- Физикальное исследование. Акцент делается на состояние периферических лимфоузлов, брюшной полости, печени, селезёнки.
- Общий анализ крови с подсчетом лейкоцитарной формулы (исключить выполнение биопсии у людей с хроническим лимфолейкозом, лейкозом острой стадии, или коклюше).
- Биохимия крови. Проводят печеночные пробы, оценивают функцию почек, уровень фермента лактатдегидрогеназы и β2 –микроглобулина.
- КТ органов грудной, брюшной полости, малого таза. Проводится с внутривенным контрастированием.
- Биопсия лимфоузлов. Проводится гистологическое исследование, иммунофенотипирование, и по возможности — определение специфических молекулярных маркеров.
- Остеосцинтиография (при необходимости).
- Электрокардиография, эхокардиография с определением фракции выброса левого желудочка.
- При возможности — позитронно-эмиссионная томография (ПЭТ).
- Другие исследования — по потребности (КТ головного мозга, люмбальная пункция с исследованием ликвора и др.).
ПЭТ
Выполнение позитронно-эмиссионной томографии позволяет точно определить стадию лимфомы. Помимо этого, преимуществами проведения ПЭТ являются:
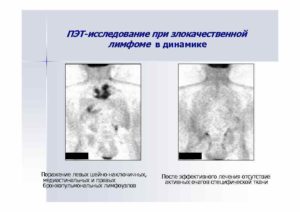
Метастазы в лимфоузлах при исследовании ПЭТ
- в сочетании с МРТ позволяет эффективно запланировать проведение лучевой терапии;
- не требует повторного проведения компьютерной томографии;
- служит отличным критерием стадийности процесса, позволяет проводить повторные исследования на всём протяжении лучевой и химиотерапии;
- позволяет охарактеризовать степень ответа опухолевого очага на проводимую терапию.
Биопсия
Во всех случаях диагноз необходимо подтверждать эксцизионной биопсией доступных лимфоузлов с гистологическим и иммуногистохимическим исследованием.
Материал аспирационной биопсии не может быть использован для установления диагноза; материала должно быть достаточно для иммунофенотипирования и генетических исследований, необходимых для диагностики и выявления прогностических онкомаркеров.
Биопсия костного мозга из подвздошной кости обеспечивает получение необходимой информации. Её следует проводить регулярно. Диагностическая ценность двусторонней биопсии костного мозга несколько выше (на 15%), чем односторонней.
Первичный биопсийный материал подлежит длительному хранению для сравнения (в случае рецидива) с материалом повторных биопсий для оценки трансформации и наличия прогностических онкомаркеров.
Аспирационная биопсия
Стоит отметить! У пациентов без легкодоступных периферических лимфоузлов следует проводить биопсию висцеральных – под контролем компьютерной томографии или ультразвукового исследования.
Физиакальное исследование
При данном исследовании устанавливают:
- какой характер имеет увеличение лимфатических узлов генерализованный или локальный;
- анализируют их консистенцию, подвижность, размеры;
- определяют отсутствие или наличие болезненных ощущений при пальпации;
- определяют уровень воспаленности близлежащих тканей;
- рассматривают очаги повреждения кожного покрова, также возможное присутствие других инфекционных поражений;
- устанавливают размеры селезенки.
Читайте здесь: Что такое адамантинома: особенности онкоопухоли
Кт с внутривенным контрастом
Если провести введение контраста внутривенно, это поможет установить присутствие и структуру опухолевых образований. Видимыми станут даже не заметные при нативном СКТ опухоли. Такое действие поможет сделать оценку кровотоку, рассмотреть состояние сосудов, определить патологические сужения в них, нарушения их функций.
Контрастное вещество имеет свойство накапливаться в опухолевых образованиях. Следовательно, именно оно считается последним подтверждением или отрицанием наличия недоброкачественной опухоли перед проведением биопсии.
Остеосцинтиграфия
Остеосцинтиграфия является методом исследования радионуклидов. Эта методика опирается на введение в организм человека радиофармацевтического препарата и дальнейшую его регистрацию в скелете, когда он там распространяется. Таким методом обследуется скелет. Находятся структурные или функциональные его изменения. Возможно обнаружение патологии на ранней стадии развития.
Этот метод определяет деструкцию и деминерализацию структуры кости, остеомиелит, устанавливает зарождение медленнорастущих опухолей доброкачественного характера, распространение метастазов, артропатологию.
Ход исследования:
Больному делается инъекция внутривенно. В качестве инъекции вводится радиоактивное вещество с индикатором. Тот в свою очередь расходится по организму, откладывается в костных тканях. Сканирование проводят через три часа.
Чтобы контрастное вещество впоследствии быстро вышло, больному рекомендуется накануне процедуры пить много жидкости. Перед началом манипуляции опорожнить мочевой пузырь. После проведенной манипуляции следует пить жидкость в большом количестве все последующие дни. Это способствует выведению радиоактивного препарата из организма.
Сама манипуляция длится около часа, в течение этого времени больной находится без движения на столе, так как любое движение отразится на качестве снимков.
Если врач не назначает никаких других предписаний, то после данной процедуры можно возвращаться к привычному образу жизни. Результаты снимков, диагноз и рекомендации пациент получает сразу после остеосцинтиграфии.
Лабораторные исследования
Лабораторные исследования должны включать полный анализ крови, чтобы оценить степень цитопении, которая может свидетельствовать об инфильтрации костного мозга или аутоиммунных нарушениях.
Лейкоцитарная формула крови с исследованием мазка периферической крови может указывать на лейкемизацию костного мозга.
Уровень электролитов, в том числе кальция и фосфатов, креатинина, функциональные пробы печени имеют весомое значение для определения дисфункции органов. Эти нарушения могут быть связаны со специфическим поражением лимфомой.
Повышение уровня лактатдегидрогеназы является важным прогностическим фактором и может служить индикатором трансформации индолентной лимфомы в агрессивную форму.
Оценка содержания иммуноглобулина и электрофорез сыворотки крови желательны, особенно в случае лимфоплазмоцитарной лимфомы, чтобы оценить наличие моноклональной глобулинопатии.
Криоглобулины также могут быть выявлены, особенно в случае лимфомы маргинальной зоны в сочетании с гепатитом С.
Тест Кумбса и определение ретикулоцитов могут быть показаны пациентам с анемией.
Другие обязательные исследования
Первоначальное обязательное обследование также включает компьютерную томографию органов грудной, брюшной полости, малого таза с внутривенным контрастированием. При этом особое внимание необходимо обращать на параметры объемного поражения и количество пораженных участков.
Обследование желудочно-кишечного тракта и биопсия подозрительных участков показаны в случаях лимфомы из клеток зоны мантии и экстранодальной мукозоассоциированной лимфомы из клеток маргинальной зоны (MALT-лимфома).
Биопсия печени может быть показана в случае выявления аномальных участков КТ-изображений или отклонений в основных лабораторных параметрах.
Нижняя лимфангиоаденография
Является одной из методик, позволяющих, с определенной точностью, найти метастазы, расположенные в лимфоузлах. Его широкую применимость в клинической практике ограничивает сложность и инвазивность. Состояние лимфатических коллекторов по результатам данного метода оценить не получается. В половине случае удается контрастировать подчревные лимфатические сосуды.
Эффективными критериями в оценке наличия метастазов рака экстранодального происхождения – является чётко контурированный дефект наполнения, с краю узла, вогнутой формы. Возможно также не очень отчётливое контрастирование группы лимфоузлов, или ассиметричное распложение лимфатических сосудов.
В любом случае, в современной диагностике данное исследование уже не используется, и диагноз устанавливается на основании информации, полученной при тазовой флебографии, томографии таза, компьютерной томографии.
Диагностика в стадировании лимфом
Для стадирования используются рентгенологические и морфологические методы, по мере внедрения новых технологий происходит естественная замена методами, более специфичными каждому типу лимфом.
Нижнюю лимфангиоаденографию полностью сменила компьютерная томография. Появление новых диагностических возможностей, таких, какие предоставляет позитронно-эмиссионная томография, приводит к ее внедрению как в первичную диагностику и стадирование, так и в оценку ответа на лечение и подтверждение факта рецидива.
Накопленные за время использования различных методик, данные уточняются, и корректируются показания к применению тех или иных методов исследования. Так, позитронно-эмиссионное исследование включено в пересмотренные руководящие принципы для агрессивных лимфом, однако процесс уточнения показаний к ПЭТ продолжается.
Существует значительная неоднородность поглощения фтора-18 фтордезоксиглюкозы в зависимости от гистологической формы лимфомы.
Например, ПЭТ демонстрирует 94% чувствительность и 100% специфичность для диагностики фолликулярной лимфомы, но еще недостаточно данных, чтобы рекомендовать ПЭТ как полноценный стандарт мониторинга процесса у пациентов с лимфомами, особенно неходжкинскими.
В то же время ПЭТ имеет значительную ценность как источник дополнительной информации для подтверждения или опровержения факта рецидива у больных лимфомами.
Цитогенетический и молекулярно-генетический анализ
Клетки вируса Эйштейна — Барра
Несомненно, что в основе происхождения опухолей лежит генетический дефект. Причины этого дефекта могут абсолютно разнообразными – и каждый из них приводит к конкретному подтипу лимфомы.
К примеру, при лимфоме Беркитта имеется нарушение генов иммунной активации против вируса Эпштейна-Барр, эти гены расположены в X-хромосоме. Поэтому вирус, попавший в организм человека, имеющего такую аномалию, предрасположен к развитию лимфомы Беркитта.
Какие-либо конкретные единичные транслокации или другие типы перестроек хромосомного материала сами по себе не являются патогномоничными лимфомам. Вывод делается на основании комплексного рассмотрения всего генетического материала.
Цитогенетический анализ разумно проводить в случае подозрений на редкую форму рака лимфатических узлов, не диагностированную никакими другими методами, в том числе морфологическим и иммуногистохимическим.
Таким материалом для анализа на рак служит эксцизионный биоптат лимфоузла, либо другого пораженного органа.
В отличие от диагностической эффективности при лейкозах, цитогенетическая картина при анализе костного мозга не дает значимого результата в диагностике лимфом. Возникает нерациональная необходимость проверки множества клеток, поэтому в данном случае анализ костномозговой ткани используется крайне редко.
Проведение FISH гибридизации трепанобиоптата костного мозга также весьма неэффективно, т.к,. во-первых, этим методом располагает ограниченное число лабораторий, а во-вторых, необходимо присутствие патоморфолога для выполнения анализа именно с пораженной частью биоптата.
Помимо этого, для гибридизации требуется тонкий срез биоптата, что не позволяет проводить быстрый анализ всего объема патологического материала.
: Дифференциальная диагностика лимфатических узлов
Источник: https://znat.su/diagnostika-raka-limfouzlov.html





